肿瘤免疫治疗简史!

-01-
研究背景
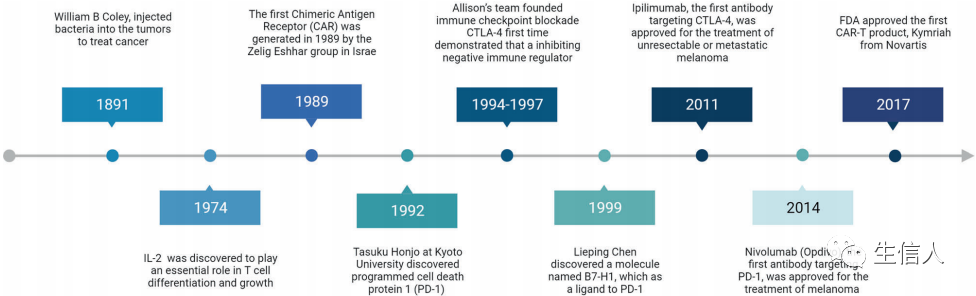
-02-
T细胞上的免疫抑制分子(ICs)
迄今为止,T细胞上其他几个通过不同机制介导抑制性信号的IC分子已被发现,并有可能被作为癌症免疫治疗的靶点加以利用。
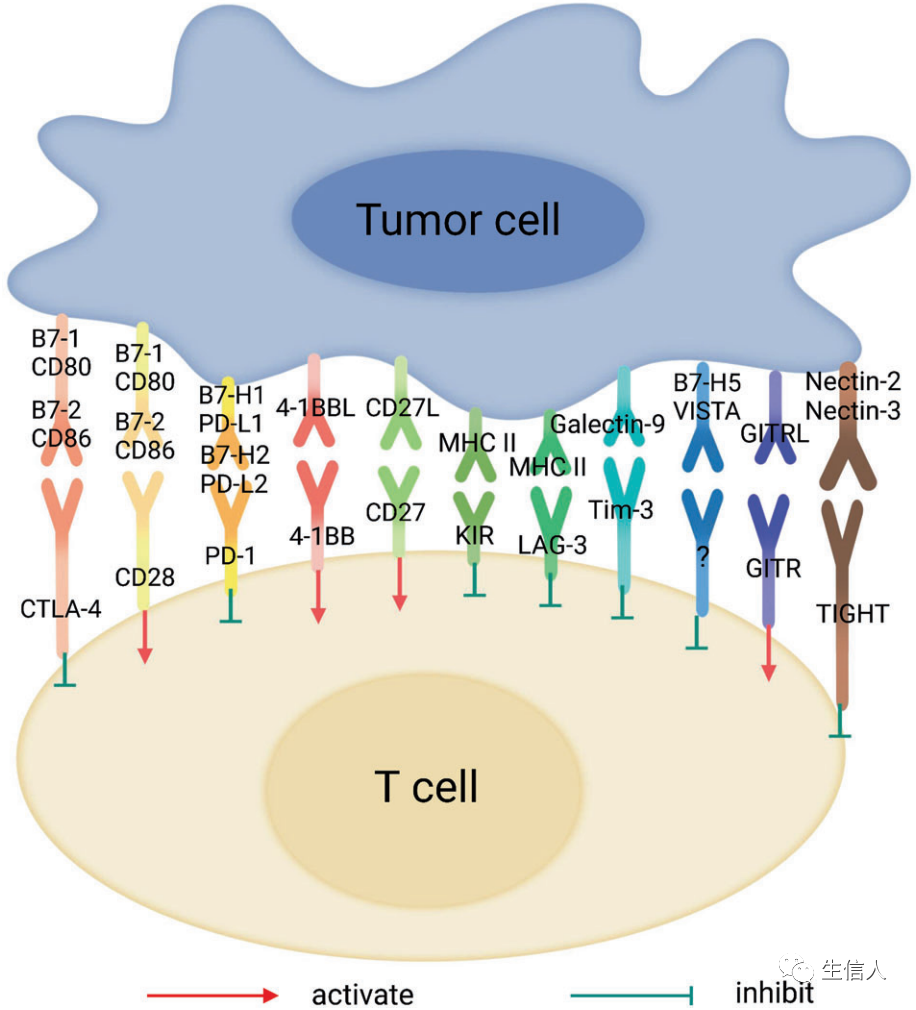
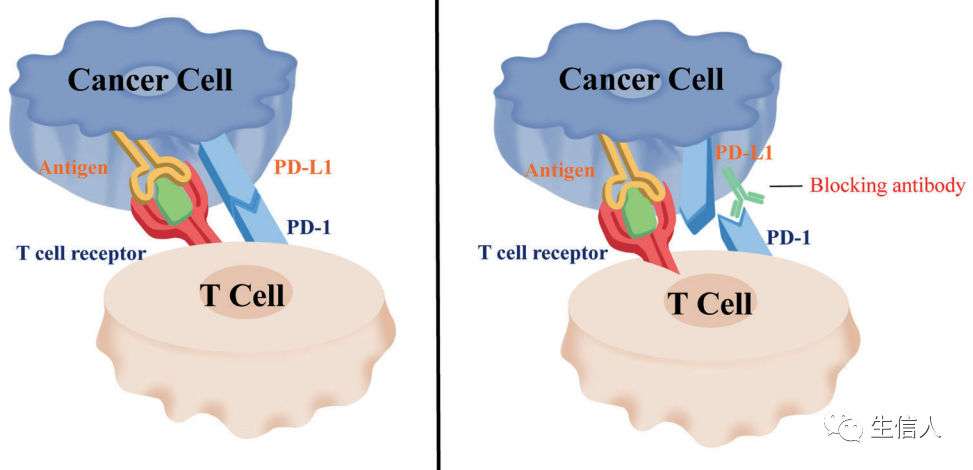
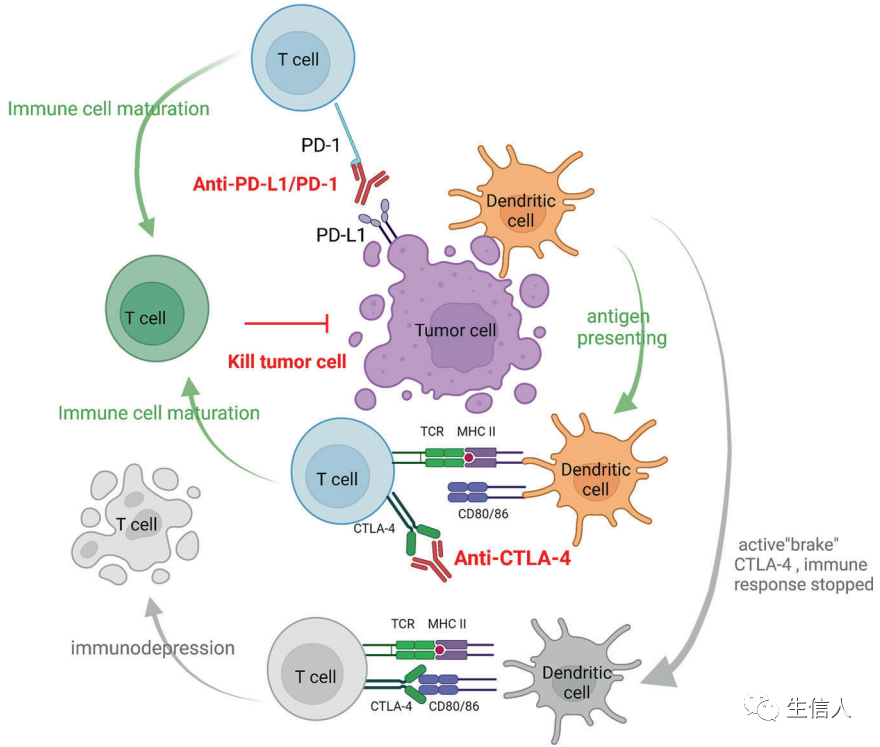 图4. CTLA-4和PD-1的图解
图4. CTLA-4和PD-1的图解
-03-
T细胞上的免疫刺激分子(ICs)
-04-
NK细胞上的免疫刺激分子(ICs)
-05-
细胞免疫治疗
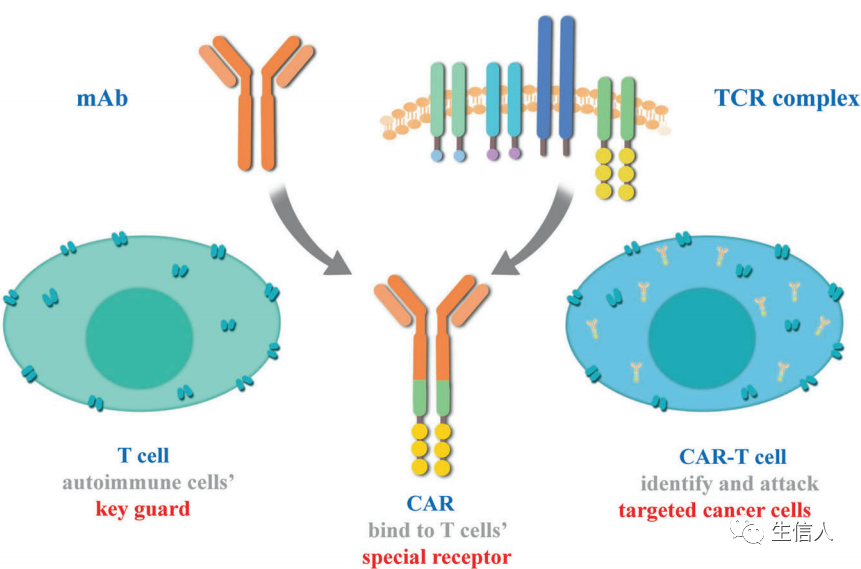
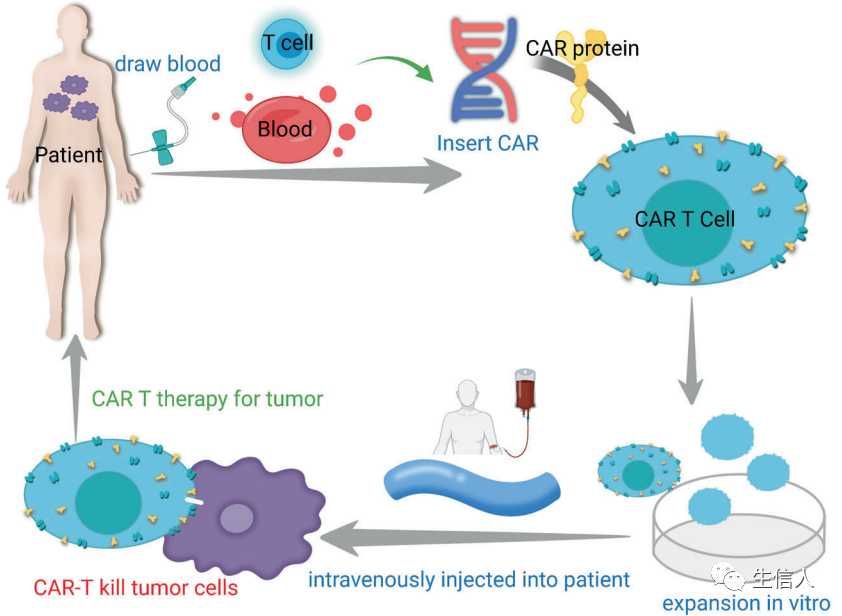 图6. CAR-T治疗的工作流程
图6. CAR-T治疗的工作流程
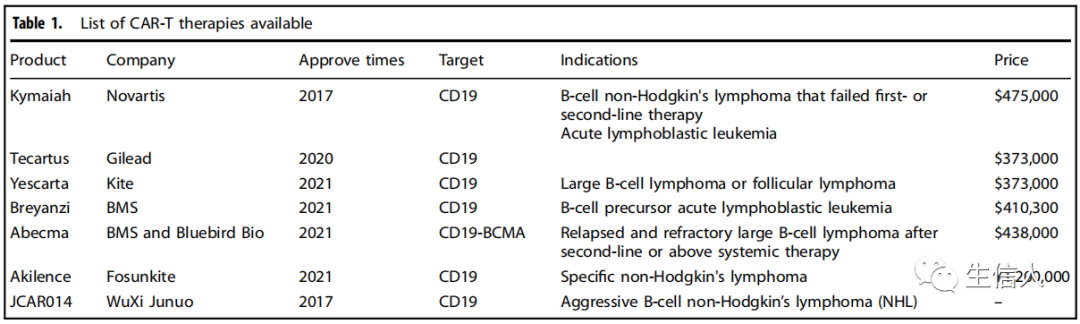
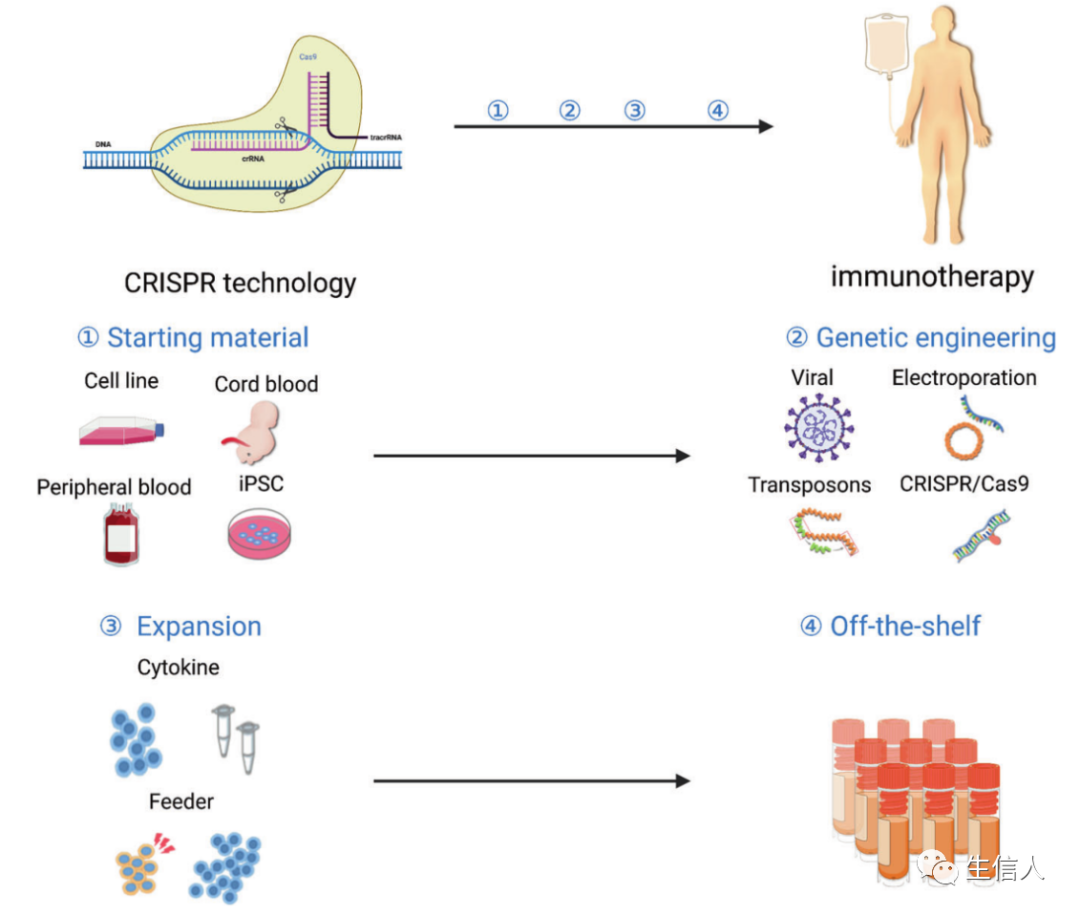
-06-
来自ICB和CAR-T细胞的免疫治疗生物标志物
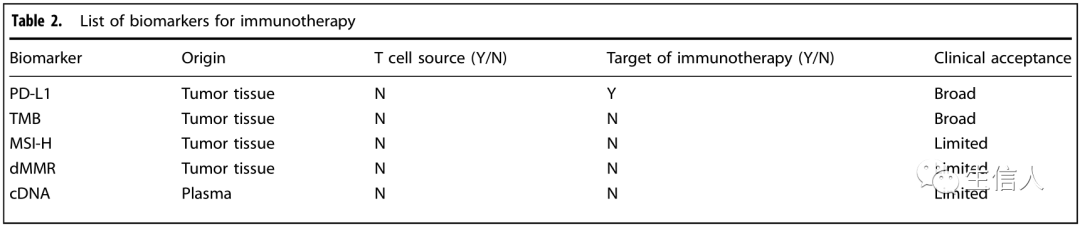
-07-
其他类型的免疫疗法
-
肿瘤疫苗: 预防性肿瘤疫苗 可以预防某些癌症的发展,包括预防宫颈癌的HPV疫苗、阴道癌、外阴癌、肛门癌和尖锐湿疣以及预防肝癌的HBV疫苗。治疗性肿瘤疫苗包括以自由肽或载于APC上的肽的形式注射肿瘤抗原,以激活免疫细胞,恢复其自主抗肿瘤能力。在临床前模型中,治疗性肿瘤疫苗已被证实可以防止癌症生长和转移,并减少终止其他类型治疗后的复发。 肿瘤疫苗主要分为以下四种:肿瘤全细胞疫苗、基因工程疫苗、蛋白肽疫苗和树突状细胞疫苗。
-
新抗原和免疫疗法: 新抗原是存在于癌细胞上的蛋白质片段,提供了一种实现癌细胞特异性靶向的新方法。新抗原疫苗是根据患者的特定肿瘤情况定制的。 生产新抗原疫苗的一般步骤包括(1)肿瘤活检,即从患者身上提取肿瘤样本进行基因组纯化; (2)对肿瘤细胞和正常细胞的全外显子组测序,使研究人员能够寻找肿瘤细胞中独特的突变;(3)特异性新抗原的预测和筛选; (4)开发个性化疫苗,这是基于预测的新抗原,可以通过多种方法实现,包括多肽、mRNA和DC。最关键和最具挑战性的一步是患者特异性新抗原的鉴定。
-
溶肿瘤病毒: 有额外病毒感染的癌症患者通常病情恶化。然而,病毒也可以被修改为专门针对癌细胞。这些“溶瘤病毒”是通过基因组编辑和大规模筛选产生的,其解读包括对癌细胞的裂解能力,同时保留正常细胞。由此产生的溶瘤病毒抗原可以复制并随后溶解肿瘤细胞,从而向肿瘤部位释放更多的病毒颗粒。因此,小剂量的病毒可以在体内扩增。溶瘤病毒具有介导肿瘤抗原扩散的能力,可导致浸润肿瘤的淋巴细胞增多,增强了ICB治疗的抗肿瘤疗效。另一种方法是使用溶瘤病毒作为载体,结合细胞免疫治疗。通过额外的基因工程,病毒的细胞溶解功能可以被抑制,同时允许合成分子的表达。
-08-
靶向抑制性的肿瘤微环境
-
巨噬细胞: 这些先天免疫系统的“士兵”清除了受损、衰老和危险的细胞,但在癌症中,巨噬细胞促进了它们的免疫逃逸,已成为药物开发的一个重要领域。 巨噬细胞有多种功能,包括清除细胞碎片和病原体,调节炎症反应。巨噬细胞也是高度可塑性的细胞,可以根据微环境刺激和信号从一种表型转换到另一种表型。巨噬细胞的激活状态通常分为两类:M1型巨噬细胞和M2型巨噬细胞(图8)。某些M2巨噬细胞亚群参与促进肿瘤进展和介导免疫抑制。从机制上讲,已发现肿瘤将单核细胞和巨噬细胞招募到TME,并将它们极化为M2样表型。巨噬细胞靶向癌症治疗的中心目标是将肿瘤相关巨噬细胞(TAMs)重编程为促炎(抗肿瘤)亚型。
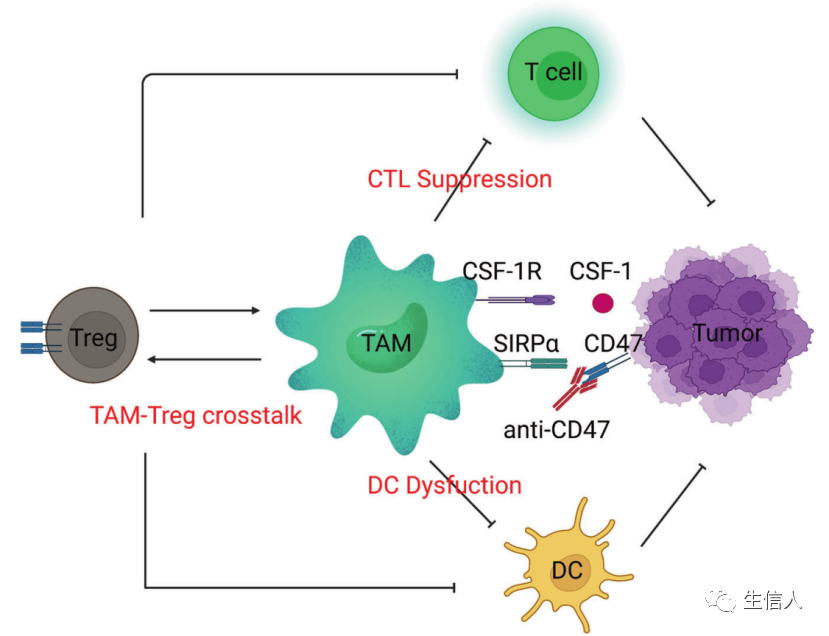
-
TAMs上的抑制和刺激分子: 最成熟的针对TAMs的方法是阻断集落刺激因子-1(CSF-1,也称为M-CSF)/CSF1R轴。这种方法减少了TAMs的数量,这也可能与TAMs向M1表型的再极化有关。TAMs的致瘤功能也可以由TGF-β介导,TGF-β是一种抗炎分子,通常在损伤修复过程中由巨噬细胞表达。在一个小鼠模型中,阻断TGF-β并同时用STING激动剂治疗,通过上调I型干扰素的表达而导致肿瘤的消退。Toll样受体(TLRs)参与先天免疫感应。TLR激动剂可以增加单核细胞的招募/浸润,并诱导巨噬细胞向促炎症表型重新极化。TAMs也表达CD40,CD40激动剂可以防止肿瘤生长和减弱抗药性。
-
工程巨噬细胞: 巨噬细胞治疗的发展需要增加靶向激活受体和更持久的M1巨噬细胞极化方法 。利用基因修饰增强巨噬细胞的抗肿瘤能力逐渐引起了人们的关注。一个直接的策略是耗尽抑制信号,如SIRPα。SIRPα缺失的巨噬细胞在联合放疗中具有抗肿瘤作用。另一种方法是设计巨噬细胞表达CARs (CAR-Ms)(图9)。CAR-Ms还诱导周围TME的促炎特征。M2巨噬细胞的存在不影响CAR-M细胞的肿瘤杀伤能力,突出了其对TME免疫抑制的抵抗力。此外,CAR-Ms表现出更强的T细胞刺 激能力,能够在吞噬后向T细胞呈递抗原,招募静止和激活的T细胞到肿瘤。
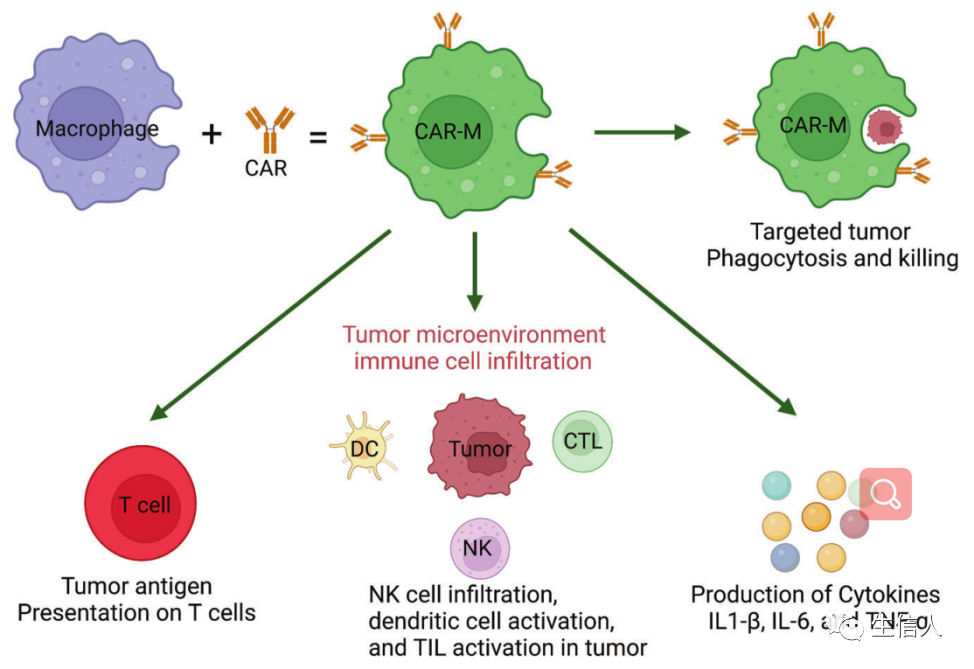
-
靶向骨髓来源抑制细胞(MDSCs): MDSCs起源于造血干细胞(HSCs),是骨髓造血功能改变的结果。这种短暂的骨髓增生在刺激物被移除后会终止,骨髓细胞的平衡也会随之恢复。然而,在慢性炎症、癌症和自身免疫性疾病中,持续的骨髓造血可能发生,以防止宿主广泛的组织损伤,不断产生IMCs。这些细胞具有明显的特征,如不成熟的表型和形态,相对较弱的吞噬功能,以及抗炎和免疫抑制功能。异常的骨髓细胞对其他免疫细胞有抑制作用。此后,人们采用表面标志物Gr-1和CD11b来定义这些免疫抑制性骨髓细胞。在人类中,这些骨髓细胞的表型特征是CD34、CD14和CD15的表达,功能特征是它们能够抑制T细胞的激活。MDSCs是指一组异质细胞,可大致分为粒细胞(G-MDSCs或PMN-MDSCs)和单细胞(M-MDSCs)亚型。MDSCs的存在是肿瘤进展的基本特征之一。 MDSCs发挥多种功能,影响T细胞、Treg细胞、DC细胞和NK细胞(图10)。 目前,MDSC靶向治疗大致可分为五种类型:(i) 抑制MDSCs扩张和招募的疗法;(ii) 恢复正常骨髓分化的疗法;(iii) 针对MDSCs上IC分子的疗法;(iv) 阻断MDSCs分泌的抑制性分子的疗法;(v) 直接耗尽MDSCs的疗法。
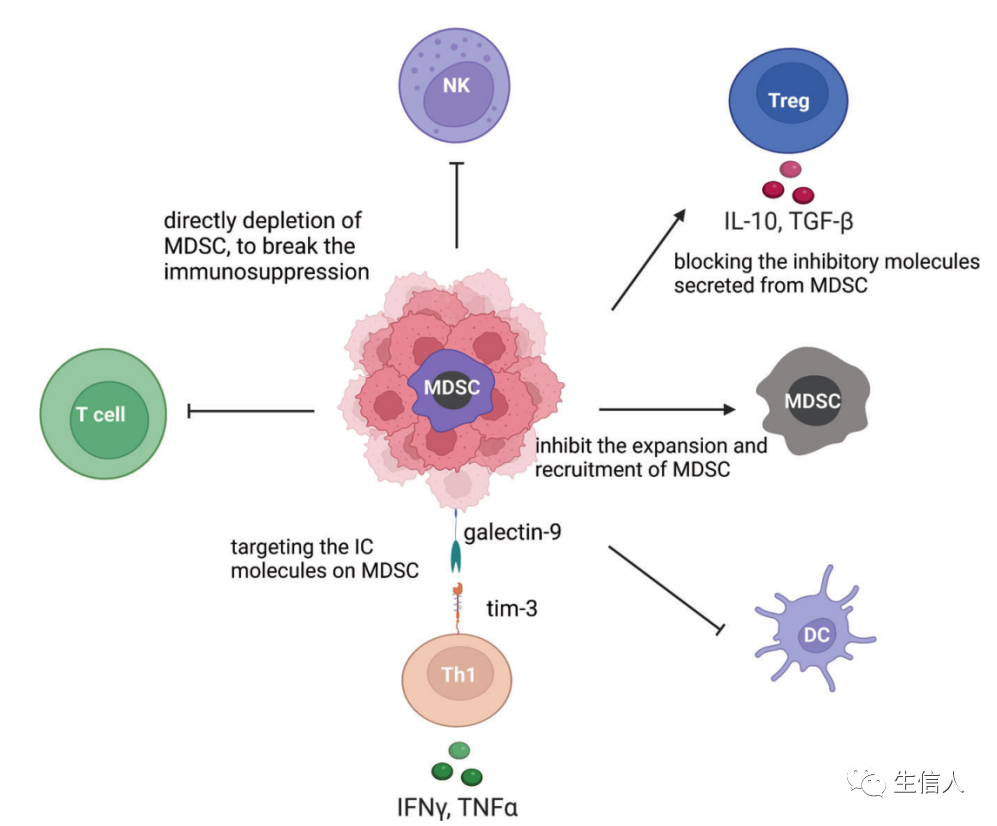
-
靶向B细胞: 肿瘤相关B细胞(TABs)。肿瘤环境中的B细胞(命名为TABs)同时具有促炎和抗炎功能,抗炎B细胞的丰富程度与黑色素瘤对ICB治疗的耐药性相关。TAB在肿瘤组织中的第三淋巴组织结构(TLSs)中富集,在那里它们可以被激活来识别癌细胞。肿瘤中TLSs中B细胞水平高的NSCLC患者更有可能对免疫治疗产生良好反应。
IDO是一种色氨酸代谢酶,可将色氨酸转化为犬尿氨酸,并在多种类型的肿瘤中过度表达。肿瘤抑制基因BIN1对IDO的表达有负向调节作用。在小鼠模型中,BIN1的耗尽已被证实能诱导IDO的表达和对肿瘤的免疫抑制。IDO可以增强癌细胞的运动能力,抑制肿瘤靶向T细胞的增殖和功能。IDO靶向药物在临床前模型中作为单药显示出疗效,但与靶向CTLA-4或PD-1/PD-L1的ICB联合使用可以更有效。目前主要有四种针对IDO的小分子抑制剂正在进行临床研究:indoximod、navoximod、epacadostat和BMS-986205。IL-41可增强肿瘤的侵袭性,抑制抗肿瘤免疫。靶向IL-41可能是一种新的免疫治疗途径。腺苷(Adenosine)是RNA合成的重要组成部分。然而,腺苷也被证明可以抑制T细胞在TME中的功能。CD39是一种参与细胞外腺苷产生的酶,在各种人类肿瘤中高度表达。此外,TME中CD39表达水平升高的多种细胞类型包括血管内皮细胞、成纤维细胞和一些免疫细胞。CD39已被发现在多种免疫细胞中发挥重要作用。因此,CD39联合ICB可能成为一种新的肿瘤免疫治疗方式。
-09-
结论和展望
这篇文章介绍了肿瘤免疫治疗的历史,深入探讨了癌症免疫治疗的不同策略,包括IC和刺激性分子靶向药物、细胞免疫治疗和抑制性TME靶向策略。此外,作者还讨论了与ICB和CAR-T治疗的临床疗效相关的生物标志物。总之,肿瘤免疫学研究与免疫细胞的先进技术相结合,将为癌症免疫治疗的未来发展指明方向。癌症免疫治疗的发展需要更多的临床和基础研究项目的整合,从而能够全面分析未满足的临床需求,进而指导研究方向。
参考文献:
Wang DR, Wu XL, Sun YL. Therapeutic targets and biomarkers of tumor immunotherapy: response versus non-response. Signal Transduct Target Ther. 2022 Sep 19;7(1):331. doi: 10.1038/s41392-022-01136-2. PMID: 36123348; PMCID: PMC9485144.
E.N.D

往期文章推荐:
资本从互联网向生物技术迁移,未来10年,细胞、基因和生物工程成为核心驱动力!
2万字收藏版:上海张江 V.S. 苏州工业园区的生命科学产业
细胞基因治疗CDMO行业深度研究报告:细胞基因疗法千帆竞发,研发生产外包踏浪前行
国内AAV基因治疗进入爆发前夕,17款IND获批,1款进入3期临床试验
北京经济技术开发区发布新政:促进细胞与基因治疗等产业高质量发展
世界首个CRISPR基因编辑疗法上市申请获受理,来自诺奖团队

